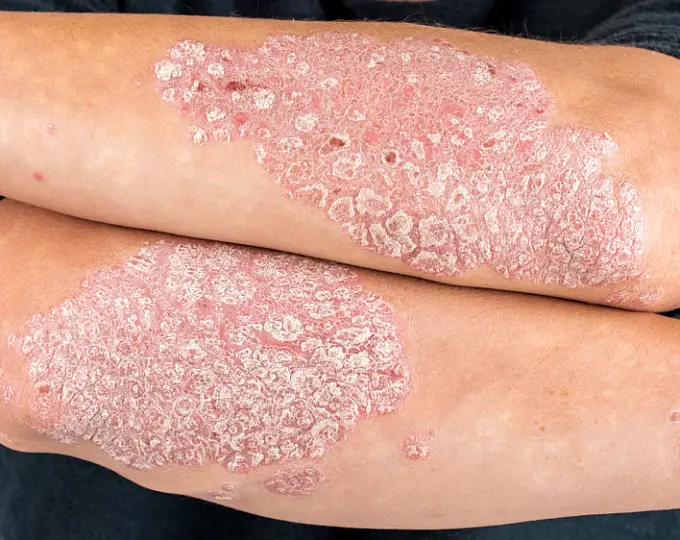
Биологический препарат бимекизумаб одобрен для лечения псориаза
Агентство по контролю за продуктами и лекарствами США (FDA) дало зеленый свет препарату бимекизумаб для терапии псориаза средней или тяжелой формы у взрослых.
Бимекизумаб блокирует действие интерлейкинов 17A и 17F.
Препарат выпускается в виде шприцов для подкожного введения. Рекомендуемая доза — 320 мг (две инъекции по 160 мг) в нулевую неделю, затем на 4, 8, 12 и 16 неделе, после чего — каждые 8 недель. Для пациентов весом 120 кг и более доза составляет 320 мг каждые 4 недели после шестнадцатой недели.
Эффективность
- Доказательством эффективности препарата послужили результаты трех рандомизированных исследований третьей фазы.
- Более 80% участников исследования достигли 90% и более улучшения по шкале PASI уже к 16 неделе.
- Улучшение на 75% (PASI 75) отмечалось у более чем 70% пациентов на 4 неделе.
Безопасность
- Самыми распространенными побочными эффектами (встречающимися менее чем у 1% пациентов) являются инфекции верхних дыхательных путей, головные боли, поражения, вызванные грибком тинеа, гастроэнтерит, простой герпес, акне и утомление.
- FDA указывает на возможное повышенное риско суицидальных мыслей/поведения, хотя прямая связь с препаратом не установлена. Важно мониторить состояние пациентов на предмет ухудшения симптомов депрессии.



